Корекція високого астигматизму за допомогою торичної інтраокулярної лінзи в очах з пересадженою рогівкою

Автори: Ali Devebacak, Cumali Degirmenci, Ozlem Barut Selver, Melis Palamar, Sait Egrilmez
Джерело: https://journals.sagepub.com/doi/full/10.1177/11206721221123885
Мета
Оцінити результати імплантації торичної інтраокулярної лінзи (ІОЛ) під час операції з видалення катаракти в очах з високим регулярним астигматизмом, пов’язаним із попередньою проникною кератопластикою (ПК).
Методи
Ретроспективний аналіз даних пацієнтів із попередньою ПК, яким було проведено неускладнену хірургію катаракти з використанням гідрофобної торичної однокомпонентної ІОЛ (EyeCryl Toric®, Biotech Vision Care, Luzern, Швейцарія).
Результати
У дослідження було включено 18 очей 18 пацієнтів. Середній вік становив 53,4 ± 12,4 (25-70) років. Середній період спостереження становив 15,5 (4-24) місяці. Середня гострота зору з найкращою корекцією (BCVA) значно збільшилася з 1,36 ± 1,0 logMAR до 0,31 ± 0,17 logMAR (p < .001) до та після операції через 4 тижні, відповідно. Протягом наступного спостереження значної зміни середньої BCVA не відбулося; середня BCVA склала 0,32±0,17 logMAR під час останнього візиту. Середній топографічний астигматизм до операції становив 652 ± 180 діоптрій (D). Середній рефракційний астигматизм зменшився з 6,55±1,62 D до 2,80±1,43 D (p0,001). Середній хірургічно індукований астигматизм (SIA) становив 3,74±0,77 D за даними векторного аналізу. Не було жодного пацієнта з відторгненням або невдачею трансплантата, середній рівень втрати ендотеліальних клітин становив 12,75±3,76% (7-17%). Не було жодного пацієнта, якому знадобилася репозиція ІОЛ.
Висновки
Імплантація торичних ІОЛ під час операції з видалення катаракти надає можливість корекції астигматизму в очах після ПК із високим регулярним астигматизмом. При виборі відповідних пацієнтів це безпечний метод, що дозволяє досягти значного покращення гостроти зору та астигматизму.
Вступ
Залишковий астигматизм після операції кератопластики (ПК), що промикується – звичайне явище. Хоча трансплантат прозорий, високий астигматизм може призвести до значної втрати зору. Існує кілька хірургічних або нехірургічних варіантів, щоб правильно керувати астигматизмом після операції кератопластики. Корекція за допомогою окулярів або контактних лінз може бути нестерпною. По можливості астигматизм слід спочатку коригувати на рогівці за допомогою рогівкових рефракційних процедур, таких як астигматична кератотомія, фоторефракційна кератектомія (PRK) або лазерний кератомілез in situ (LASIK). Факічні торичні інтраокулярні лінзи (ІОЛ) є ще одним прийнятним варіантом лікування для пацієнтів, яким ці рогівкові процедури протипоказані. Хірургія катаракти з торичними ІОЛ може розглядатися у випадках, коли ці процедури не можуть бути виконані, у випадках із зорово значущою катарактою, у пацієнтів віком від 50-55 років. Так, утворення катаракти відбувається відносно швидше у пацієнтів із кератопластикою внаслідок тривалого застосування топічних кортикостероїдів. З іншого боку, хірургія катаракти з торичними ІОЛ на сьогодні є визнаним варіантом, який не впливає на анатомічну цілісність рогівки, що є значною перевагою.
10-річне виживання трансплантата може досягати 88%, залежно від первинного захворювання, що призвело до пересадки рогівки. У разі невдачі трансплантата існують такі варіанти, як заміна ендотелію замість повної заміни трансплантата. Тому в таких очах важливо скоригувати залишковий астигматизм, пов’язаний із трансплантацією. Коли потрібна операція видалення катаракти, торичні ІОЛ можуть бути хорошим вибором для зменшення залишкового астигматизму та сферичних помилок.
Метою цього дослідження було оцінити результати імплантації торичних ІОЛ під час операції з видалення катаракти у пацієнтів із ПК із високим астигматизмом.
Матеріали та методи
Був проведений ретроспективний аналіз даних пацієнтів із попередньою ПК, яким у період із січня 2016 року до вересня 2019 року було проведено неускладнену хірургію катаракти з використанням гідрофобної торичної ІОЛ (EyeCryl Toric®, Biotech Vision Care, Luzern, Швейцарія).
Дослідження відповідало принципам Гельсінської декларації, і Комітет з інституційної етики Університету Еge схвалив це дослідження.
Усі пацієнти, яким були проведені ПК з прозорим трансплантатом, візуально значущою катарактою, повним зняттям швів не менше ніж за 6 місяців до операції, значною мірою ортогональним і симетричним залишковим астигматизмом на топографії рогівки (рис. 1), спостереженням протягом не менше 4 місяців після операції катаракти, повними клінічними та хірургічними даними, були допущені до цього дослідження.
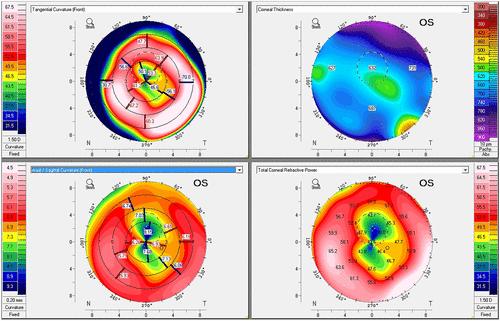
Мал. 1. Схематична візуалізація (Pentacam, Oculus, Німеччина) очей з кератопластикою, що промикується, з відносно регулярним рогівковим астигматизмом і малюнком «бантик»
Записи пацієнтів були вивчені щодо віку, статі, показань до кератопластики, рефракції до та після операції, значень кератометрії до та після операції, отриманих за допомогою топографії рогівки Scheimpflug (Pentacam, Oculus Optikgeräte GmbH, Wetzlar, Німеччина), втрати ендотеліальних клітин (CEM) -530, NIDEK Co, Ltd (Японія), часу спостереження, прозорості трансплантата, гостроти зору без корекції (UCVA) до та після операції, гостроти зору з найкращою корекцією (BCVA) до та після операції (за таблицею Снеллена).
Для визначення осьової довжини використовувався прилад оптичної біометрії (Al-Scan; NIDEK Co. Ltd., Гамагорі, Японія). Рефракційна сила торичних ІОЛ розраховувалася за допомогою онлайн-програми виробника (Eyecryl Toric Calculator, Biotech).
Лімбальні точки 0 і 180 відзначалися, коли пацієнт сидів біля щілинної лампи. Для всіх операцій використовувалася місцева анестезія. Розріз рогівки виконувався через супратемпоральну ділянку для правого ока та супраназальну ділянку для лівого ока (триступінчастий; прозора рогівка; 2,75 мм). Всім пацієнтам було проведено звичайну операцію факоемульсифікації та ІОЛ була імплантована у капсульний мішок. Наприкінці операції обертальне положення ІОЛ перевірялося після аспірації віскоеластичного пристрою.
Значення астигматизму розраховувалися як чисельним, так і векторним методом. Векторний аналіз проводився методом Альфінса. Вектор хірургічно індукованого астигматизму (SIA), що також враховує потужність ІОЛ, означає діапазон досягнутої корекції астигматизму в результаті операції.
Значення BCVA та рефракції до операції, через місяць після операції й під час останнього візиту були отримані на основі суб’єктивної корекції при фізичному огляді відповідно до топографічних та явних вимірів рефракції. Стан ротації ІОЛ контролювався за допомогою щілинної лампи після розширення зіниці на післяопераційних візитах.
Статистичний аналіз проводився за допомогою програмного забезпечення SPSS для Windows версії 15.0 (SPSS Inc, Чикаго, Іллінойс, США) та Microsoft Office Excel (Microsoft, Редмонд, Вашингтон, США). Статистичний аналіз проводився з допомогою парних вибіркових t-тестів. Значення p<0,05 приймалося як статистично значуще.
Результати
У дослідження було включено 18 очей 18 пацієнтів (5 жінок, 13 чоловіків). Середній вік становив 53,4 ± 12,4 (25-70) років. Усі пацієнти з попередньою пересадкою рогівки мали чисті трансплантати та повне зняття швів не менше ніж за 6 місяців до операції з видалення катаракти. Показання до кератопластики були такими: кератоконус, дистрофія рогівки, рогівка, пеллюцидна крайова дегенерація, кератоглобус. Середній період спостереження після операції з видалення катаракти становив 155 ± 68 (4-24) місяців.
Збільшення BCVA спостерігали у всіх пацієнтів. Доопераційна середня BCVA становила 1,36 ± 1,0 (0,3-3,1) logMAR, а післяопераційна середня BCVA на 4-му тижні – 0,31 ± 0,17 (0,05-0,7) logMAR (p0001). Протягом наступного спостереження відмічалася значна зміна середньої гостроти зору; середня BCVA склала 0,32±0,17 logMAR під час останнього візиту (рис. 2). Середнє значення UCVA до та після операції на 4-му тижні склало 2,12 ± 0,72 (1,3-3,1) та 0,79 ± 0,38 (0,2-1,3) logMAR, відповідно (p0001).
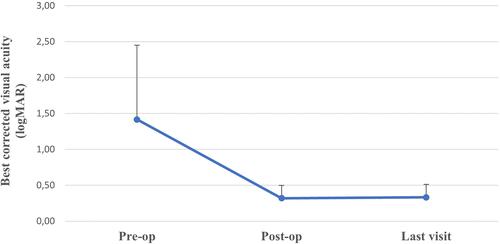
Рис. 2. Підвищення гостроти зору з найкращою корекцією (BCVA) спостерігалося у всіх пацієнтів. До операції середня BCVA становила 1,36 ± 1,0 logMAR, а після операції на 4-му тижні BCVA склала 0,31 ± 0,17 logMAR (p0,001). Протягом наступного спостереження значних змін BCVA не відбулося; середня BCVA склала 0,32 ± 0,17 logMAR під час останнього візиту
У всіх пацієнтів спостерігалося зменшення вираженого рефракційного астигматизму. Середній топографічний астигматизм до операції становив 652 ± 180 D (рис. 3). Середній рефракційний астигматизм становив 6,55 ± 1,62 D та 2,80 ± 1,43 D на доопераційному та післяопераційному візитах на 4-му тижні, відповідно (p 0,001). Середній рефракційний астигматизм становив 2,88±1,26 D на останньому візиті. Не було значних змін у середньому рефракційному астигматизмі між післяопераційним місяцем та останнім візитом (p > 0,05). Середнє значення сферичного еквівалента склало -1,06 D (SD = 1,76 D) на 4-му тижні після операції.
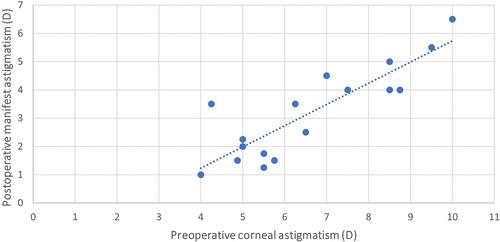
Рис. 3. Показано доопераційні топографічні та післяопераційні значення явного астигматизму. D = діоптрії
При векторному аналізі було зазначено, що було отримано значну корекцію астигматизму (рис. 4). Середня величина SIA становила 3,74±0,77 D.
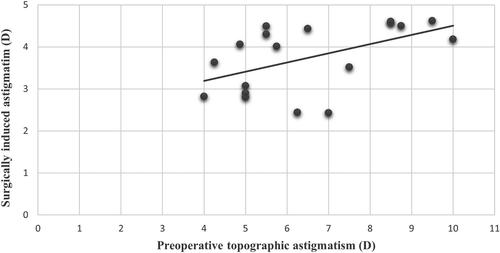
Рис. 4. Доопераційні значення топографічного астигматизму та значення хірургічно індукованого астигматизму, розраховані за допомогою векторного аналізу. Середній хірургічно індукований астигматизм становив 3,74±0,77 D
Під час спостереження у жодного з пацієнтів не було виявлено відхилення осі ІОЛ більш ніж на 5°. Не було жодного пацієнта з відторгненням чи невдачею трансплантату. У пацієнтів, у яких ендотеліальні клітини до та після операції через місяць можна було підрахувати за допомогою спекулярної мікроскопії (CEM-530, NIDEK Co., Ltd., Японія), середній рівень втрати ендотеліальних клітин становив 12,75±3,76% (7-17%). У післяопераційному періоді не було жодного пацієнта із внутрішньоочною гіпертензією.
Обговорення
Астигматизм, спричинений ПК, є очікуваним результатом операції. Існують різні рогівкові процедури, такі як селективне зняття швів, астигматична кератотомія, PRK, LASIK, що можуть бути виконані на початковому етапі для корекції астигматизму після ПК. Імплантація торичної ІОЛ відрізняється від цих методів, оскільки це некорнеальна процедура. Вона є цінною альтернативою, коли цим пацієнтам потрібна операція з видалення катаракти.
У цьому дослідженні, як і очікувалося, астигматизм з явною рефракцією зменшився. Ефективність операції підтверджувалася результатами векторного аналізу. Стабільність цих вимірів спостерігалася під час спостереження в усіх пацієнтів. Ці результати свідчать про ефективність торичних ІОЛ для хірургічної корекції астигматизму в очах після ПК. У літературі повідомлялося, що імплантація торичних ІОЛ при залишковому астигматизмі після ПК дала прийнятні рефракційні результати з відмінною стабільністю ІОЛ. Втрата ендотеліальних клітин через місяць після операції з видалення катаракти склала 19,03%. Аналогічно до цього результату, у цьому дослідженні втрата ендотеліальних клітин склала 12,75 ± 3,76%. Ці результати показують, що хірургія катаракти з імплантацією торичної ІОЛ у пацієнтів з попередньою ПК не відрізняється від звичайної хірургії катаракти з точки зору втрати ендотеліальних клітин.
З іншого боку, середній післяопераційний залишковий астигматизм у цьому дослідженні становив 2,8 D. Причину такого залишкового астигматизму можна пояснити тим, що середній рогівковий астигматизм (6,5 ± 1,8 D) був вищим за верхню межу (4,11 D) торичної ІОЛ (Biotech Eyecryl HFY-60), використаної у дослідженні. Вибір торичної ІОЛ був зроблений відповідно до марки лінз, що є в установі. Тому замість неторичної ІОЛ ми віддали перевагу використанню цієї торичної ІОЛ для зниження вищих астигматичних значень до більш терпимих рівнів. Значення SIA 3,74±0,77 D вказувало на відсутність значної недокорекції. Оскільки в оцінці ефективності слід враховувати очікуваний результат, можна дійти невтішного висновку, що цільову корекцію астигматизму практично досягнуто. На 4-му тижні після операції середній сферичний еквівалент становив -1,06 D (SD = 1,76 D). Широкий діапазон цього значення може бути пов’язаний з можливими помилками у біометричних вимірах в очах після ПК через труднощі, пов’язані з трансплантатом, таких як нерівність поверхні рогівки.
В очах після ПК можна коригувати астигматизм під час операції з приводу видалення катаракти за наявності значного візуального помутніння кришталика. Найважливішим питанням щодо цього є відбір пацієнтів. Необхідно знати вихідні захворювання рогівки, що призвели до пересадки рогівки. Торичні ІОЛ можуть не підійти у випадках, коли астигматизм може значно змінитися, наприклад, при ектазії. Однак для таких пацієнтів також важливим є час операції. Рогівкові шви повинні бути зняті не менше ніж за 6 місяців до операції з приводу видалення катаракти, при цьому має спостерігатися стабільний рогівковий астигматизм. Астигматизм після кератопластики в основному нерегулярний, що неможливо виправити за допомогою імплантації торичної ІОЛ. Тому лише пацієнти з регулярним компонентом у загальному рогівковому астигматизмі мають розглядатися для цього варіанту лікування. Топографія рогівки повинна мати симетрію не менше 2/3.6.
Однією з головних проблем після імплантації торичних ІОЛ у вічі після ПК є майбутня необхідність повторної кератопластики з будь-якої причини. Новий рогівковий трансплантат, особливо повної товщини, може викликати плутанину рефракції під дією торичної ІОЛ. За такого сценарію було б розумно провести ендотеліальну кератопластику наявного трансплантату рогівки, якщо це можливо, щоб мінімізувати зміну астигматизму.
Хоча у жодного пацієнта в ході періоду спостереження у цьому дослідженні не відбулося руйнування трансплантата, у майбутньому для таких очей може знадобитися повторна кератопластика та навіть операція із заміни ІОЛ. Як і очікувалося, у літературі не так багато даних із цього питання. Заміна ІОЛ не буде проблемою, якщо капсула інтактна та є правильний циркулярний отвір капсули. Тому при підозрі на пошкодження капсули під час первинної хірургії катаракти доцільно використовувати неторичні ІОЛ замість торичних ІОЛ. Відповідно, навіть якщо в таких очах під час післяопераційного спостереження розвивається заднє капсулярне помутніння, слід по можливості уникати капсулотомії та зберігати цілісність капсули.
З іншого боку, ІОЛ «piggy-back», що легко видалити за потреби, можуть розглядатися як первинний варіант у цих пацієнтів. При захворюваннях рогівки існує ймовірність того, що післяопераційний астигматизм не буде стабільним у довгостроковій перспективі. Тому ці процедури можуть знадобитися у майбутньому, навіть якщо не станеться руйнування трансплантата.
У підсумку варто зазначити, що коли потрібна операція з приводу видалення катаракти в очах після ПК, імплантація торичної ІОЛ є гарним варіантом, оскільки регулярний астигматизм може бути скоригований без впливу на структуру трансплантата. При відносно великій кількості пацієнтів і тривалому періоді спостереження було показано, що гострота зору та астигматизм у цих пацієнтів стали значно кращі. Несподівані рефракційні результати можуть виникнути через пов’язані з трансплантатом труднощі при вимірюванні осьової довжини та кератометрії. Його слід уникати в очах з імунологічними чинниками ризику відторгнення, такими як наявність запалення, герпетичного захворювання очей і глибокої стромальної неоваскуляризації рогівки.

 0(67) 551 50 02
0(67) 551 50 02